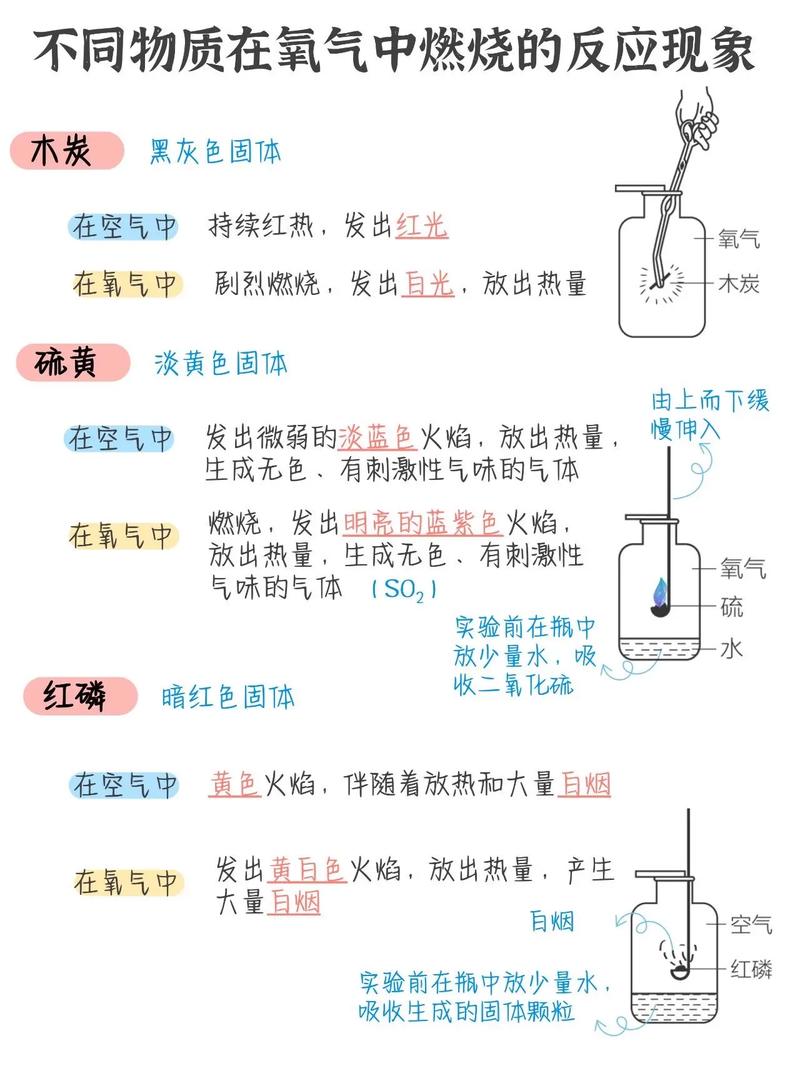
白磷燃烧是一个化学过程,主要涉及白磷(P4)与氧气(O2)之间的反应。以下是白磷燃烧的基本介绍:
1. 化学性质: 白磷(P4)是一种无色或淡黄色的蜡状固体,具有剧毒。 它在常温下可以自燃,因为它的着火点非常低,大约在30°C左右。
2. 燃烧过程: 当白磷暴露在空气中时,它会迅速与氧气反应,产生磷酸酐(P4O10)和五氧化二磷(P2O5)。 这个反应是剧烈的,会产生大量的热量和光。
3. 化学方程式: 4P + 5O2 → 2P2O5
4. 应用: 白磷燃烧产生的高温和光亮使其在某些应用中非常有用,例如军事信号、烟火和某些类型的照明。 由于其剧毒性质,白磷的使用受到严格限制,并且需要遵守特定的安全规定。
5. 安全注意事项: 白磷的储存和使用需要特别的防护措施,以防止意外燃烧和暴露。 在处理白磷时,必须佩戴适当的防护装备,并确保良好的通风。
白磷燃烧是一个重要的化学现象,但在实际应用中需要非常谨慎,以确保安全。
白磷燃烧:一种危险的化学反应
白磷,这种看似普通的物质,却隐藏着巨大的危险。它是一种无色蜡状结晶体,遇光会变为黄色,在暗处发出淡绿色荧光,有大蒜臭味,剧毒。它的分子式为P4,分子量为124.08,着火点仅为40℃,相对密度为1.82g/cm3,熔点44.1,沸点280.5。白磷不溶于水,微溶于苯、氯仿,易溶于二硫化碳等有机溶剂。
白磷自燃的原因
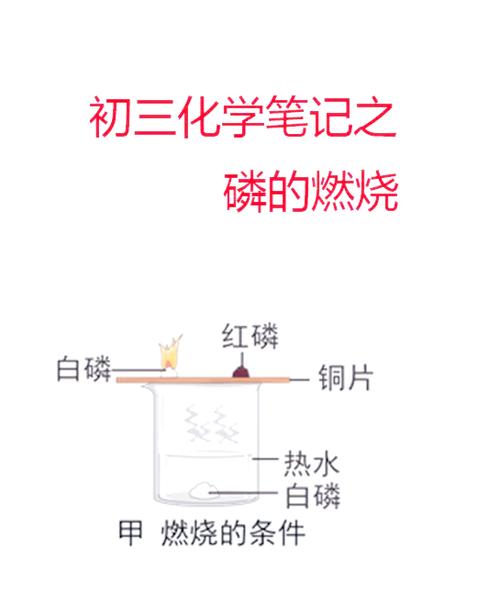
白磷对安全条件的要求特别高,在实际生产、储存、运输中,白磷不仅能发生自燃,酿成火灾,而且还容易侵入人体,造成人身伤害。白磷的火灾危险特性主要表现在:白磷属于自燃物品。常温下,白磷接触到空气即可冒烟自燃,即使当时外界温度达不到白磷的着火点,但其接触到空气后即会产生磷化反应,释放热量,自行促进燃烧。
| 白磷自燃原因 | 描述 |
|---|---|
| 与空气接触 | 白磷在常温下与空气接触即可冒烟自燃。 |
| 磷化反应 | 白磷接触到空气后即会产生磷化反应,释放热量。 |
| 撞击、摩擦 | 白磷受到撞击、摩擦或与氯酸钾等氧化剂接触后,也能立即燃烧,甚至爆炸。 |
白磷燃烧时的应急处理
白磷燃烧时应立即用清水扑灭,防止溅散;磷烧伤皮肤时,立即浸入清水中,先用2%碳酸氢钠溶液浸泡,再用1—2%CUS04溶液冲洗烧伤处,经现场应急处理后,立即送往附近医院治疗;口服黄磷中毒时立即用0.2%硫酸铜洗胃,同时禁忌脂肪食物和牛奶。
白磷的储存与取用
由于白磷非常危险,因此不能将白磷露置于空气中。根据白磷不溶于水,且比水的密度大,可以将少量的白磷放入盛有冷水的广口试剂瓶中,并经常注意保持足够的水量。通过水的覆盖,既可以隔绝空气,又能防止白磷蒸气的逸出,同时还能保持白磷处于燃点之下。不常用的白磷可以贮存于封口的试剂瓶中,并埋入沙地里。
由于白磷的燃点低,人的手温就容易使它燃烧,所以取用白磷时必须用镊子去取,绝对不能用手指去接触,否则手就会被灼烧,造成疼痛难愈的灼伤。如果遇到大块白磷需要切割成小块时,必须把它放在盛有水的水槽中,用小刀在水面下切割,绝不能暴露在空气中进行,否则切割时摩擦产生的热也容易使白磷燃烧。
白磷的用途
尽管白磷具有极高的危险性,但它在工业、军事等领域仍有着广泛的应用。例如,在工业方面可以制备高纯度磷酸,在军事方面可以用来制作烟雾弹、燃烧弹,或者是杀鼠剂等物品。
以上就是黄楼生活网小编为大家分享的白磷燃烧,白磷燃烧的化学方程式为什么不是p4「已解决」,希望对大家有所帮助,了解更多问题欢迎关注黄楼生活网!
站长不易,多多少少是点心意








